MoDC的制備
1.外周血單個核細胞的采集
1.1用血細胞分離機采集患者自身的外周血單個核細胞80-100ml�����;
1.2淋巴細胞分離液密度梯度離心法進一步純化單個核細胞(PBMC) �����。
1.3無血清培養(yǎng)液洗滌2次����, 獲得純度在90%以上的PBMC����, 細胞數(shù)量需達到1-3×10^8��。
2.(可選步驟)腫瘤抗原的制備
用于負載DC的腫瘤抗原可以是腫瘤特異性抗原肽(Tumor-Specific Ant gens��, TSA)或腫瘤相關(guān)抗原(Tumor-Associated Antigens��, TAA) �, 也可以是腫瘤全細胞抗原����。
用TSA或TAA負載的DC具有很好的靶向性, 但該方法具有已確定的腫瘤特異性抗原或抗原肽種類少和單一抗原的免疫攻擊經(jīng)常無法殺傷腫瘤細胞等缺陷�����。而用腫瘤全細胞抗原負載DC可克服這些缺陷�, 因為此時無需知道哪些抗原是腫瘤細胞的TSA或TAA, 而且全抗原中的多種不同腫瘤抗原沖擊DC可誘導(dǎo)產(chǎn)生針對不同抗原決定簇的細胞毒T淋巴細胞(CTL) 克隆����, 從而實現(xiàn)對腫瘤細胞的有效殺傷。
腫瘤細胞全抗原負載DC的方法很多,包括用腫瘤細胞裂解液負載DC����、用凋亡腫瘤細胞負載DC、用壞死或死亡的腫瘤細胞負載DC��,用腫瘤活細胞負載DC�����,和將腫瘤細胞與DC融合等�����。目前臨床上常用的是用腫瘤細胞裂解液負載DC���,因該方法簡單�����、快速���、有效。
反復(fù)凍融是獲得腫瘤細胞裂解液的常見方法��,具體步驟如下:
2.1手術(shù)切除腫瘤標(biāo)本,無菌條件下��,將壞死組織和癌旁非腫瘤組織去除干凈�����;
2.2無菌生理鹽水洗3次�����;
2.3用無菌的組織剪將腫瘤組織剪碎���, 加入RPMI 1640培養(yǎng)基, 充分研磨����;
2.4200目無菌網(wǎng)過濾后收集單細胞懸液;
2.5用RPMI 1640培養(yǎng)基重懸細胞至1-2×10/ml�����, 裝入5ml無菌凍存管中��;
2.6將凍存管浸入液氮中速凍����, 10min后取出�����, 再迅速放入37℃水浴中解凍10min��。反復(fù)3-5次
注:也可以-80C/37C反復(fù)凍融3-5次����。
2.7將腫瘤裂解物加入離心管中���, 3000rpm�����, 離心10min�����;
2.8收集上清����,0.22um濾膜過濾除菌�,留樣檢測蛋白含量及細菌�、真菌和支原體�����;
2.9-80℃保存?zhèn)溆谩?span style="white-space:pre">
3.DC細胞的培養(yǎng)及鑒定
3.1步驟1中獲得的PBMC用無血清培養(yǎng)液調(diào)整細胞濃度至2×10°/ml���, 置于培養(yǎng)瓶內(nèi)���;
3.237℃,5%CO培養(yǎng)箱中孵育2h�����,以使單核細胞貼壁�;
3.3洗去懸浮細胞���, 在貼壁細胞中加入含重組人GM-CSF(500-1����, 000U/ml) 和重組人IL-4(500U/ml)的無血清培養(yǎng)液�����,37℃,5%CO2培養(yǎng)箱中培養(yǎng)�,誘導(dǎo)單核細胞向DC細胞分化;
3.4每2-3d半量換液一次�����,并補足細胞因子�����;
3.5(可選步驟)在培養(yǎng)的第5d,加入步驟2中獲得的腫瘤抗原50ug/ml�,對DC進行抗原負載�;
注:若不對DC進行抗原負載,該步省略����。
3.6在培養(yǎng)的第6d, 加入重組人TNF-α(10ng/ml) ���, IL-1β(10ng/ml) �����, IL-6(1000U/ml) 和PGE 2(1ug/ml) �����, 誘導(dǎo)DC細胞成熟�;
3.7在培養(yǎng)的第7d或第8d,收獲DC細胞��,其數(shù)量應(yīng)達到1×10°個以上����;
3.8DC的質(zhì)檢:
3.8.1活細胞比例:臺盼藍染色驗證活細胞應(yīng)在90%以上;
3.8.2形態(tài)學(xué)觀察:>90%細胞半懸浮�����,細胞有多個樹突樣突起�;
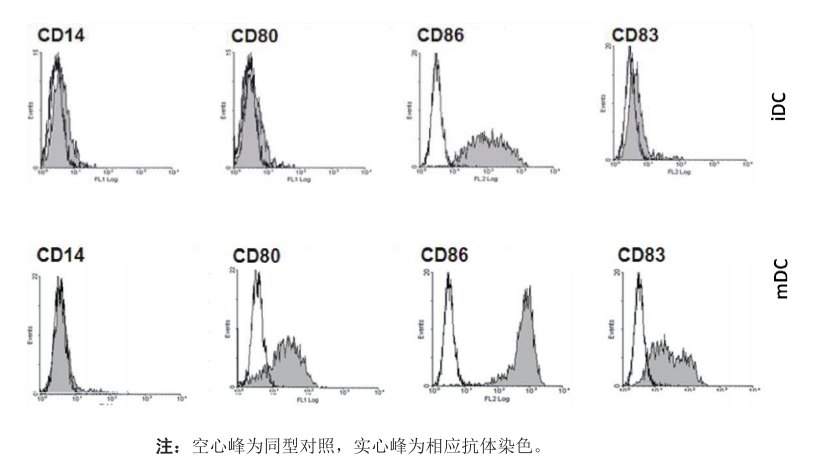
3.8.3細胞表型分析(見下圖) :流式細胞術(shù)檢測DC細胞表面CD 14、HLA-DR����、
CD40���、CD80�、CD83和CD86等分子的表達�����,成熟的DC不表達CD14,
而高表達其他分子����。CD83是成熟DC的特異性標(biāo)志,在單核細胞和不成熟
DC表面不表達或低表達����;
3.8.4無菌檢測:收獲細胞前取少量培養(yǎng)物進行細菌、真菌培養(yǎng)����,并檢測支原體、
衣原體�,均應(yīng)為陰性;
3.8.5內(nèi)毒素檢測:回輸前���,用萱試劑檢測內(nèi)毒素含量�����,標(biāo)準(zhǔn):內(nèi)毒素<0.5EU/ml�。
DC培養(yǎng)試劑推薦
| 生廠商 | 產(chǎn)品名稱 | 產(chǎn)品貨號 | 產(chǎn)品規(guī)格 | 使用濃度 |
| PeproTech | 重組人GM-CSF(Animal Free) | AF-300-03
| 5μg/20μg/50μg/100μg/250μg/500μg/1mg | 50-100ng/ml |
| PeproTech | 重組人IL-4 (nimal Free) | AF-200-04 | 5μg/20μg/50μg/100μg/250μg/500μg/1mg | 100ng/ml |
| PeproTech | 重組人TNF-α?? (nimal Free) | AF-300-01A | 10μg/50μg/100μg/250μg/500μg/1mg | 10ng/ml |
| PeproTech | 重組人IL-1β? ?(nimal Free) | AF-200-01B | 2μg/10μg/50μg/100μg/250μg/500μg/1mg | 10ng/ml |
| PeproTech | 重組人IL-6 (nimal Free) | AF-200-06 | 5μg/20μg/50μg/100μg/250μg/500μg/1mg | 100ng/ml |
PeproTech (BioGems) | PGE2(前列腺素 E2) | 3632464 | 10mg/50mg | 1ng/ml |
注:Animal Free意為無動物成分�����。無動物成分的重組細胞因子在生產(chǎn)過程中不會有任何動物源性物質(zhì), 尤其是牛的病原體和蛋白的混入��,使得最終獲得的重組人蛋白中不含任何動物成分�����。這樣可避免動物病原體(如瘋牛病����,克雅氏病等)的污染及外源蛋白引起的機體異種排斥和過敏反應(yīng),因此細胞治療的體外細胞培養(yǎng)過程中最好使用無動物成分的重組細胞因子�。
DC鑒定試劑推薦
| 生產(chǎn)商 | 產(chǎn)品名稱 | 產(chǎn)品編號 | 克隆號 | 熒光標(biāo)記 | 規(guī)格 |
PeproTech (BioGems) | 抗人CD14熒光標(biāo)記抗體 | 06211 | 61D3 | FITC/PE/APC/Per CP-Cy 5.5 | 25tests/100test |
| 抗人CD40熒光標(biāo)記抗體 | 02511 | 5C3 | FITC/APC | 25tests/100test |
| 抗人CD80熒光標(biāo)記抗體 | 02911 | 2D10.4 | FITC/PE | 25tests/100test |
| 抗人CD83熒光標(biāo)記抗體 | 05911 | HB15e | FITC/PE | 25tests/100test |
| 抗人CD86熒光標(biāo)記抗體
| 08911 | IT2.2
| PE | 25tests/100test |
| 抗人HLA-DR熒光標(biāo)記抗體 | 74111 | LN3 | FITC/PE/APC/Per CP-Cy 5.5 | 25tests/100test |
注:用于DC鑒定的表面標(biāo)志物的表達在流式圖上均呈現(xiàn)單個峰,且多數(shù)情況下不能與陰性峰完全區(qū)分開來�。為避免多色分析時補償調(diào)節(jié)不好導(dǎo)致結(jié)果的不準(zhǔn)確性,建議最好用單標(biāo)���,最多用雙標(biāo)來做DC表面標(biāo)志的分析���,而且必須使用同型對照,而非空白細胞對照來排除背景染色��。
參考文獻:
[1] Steinman RM��, Cohn ZA.Identification of a novel cell type in peripheral lymphoid organs of mice.I.Morphology�, quantita-tion, tissue distribution.J.Exp.Med.1973����; 137(5) :1142-62.
[2] Bender A, Sap pM��, et.al.Improved methods for the generation of dendritic cells from non proliferating progenitors in human blood.J Immunol Methods.1996�����; 196(2) :121-35.
[3] Roman iN��, Reider D���, et.al.Generation of mature dendritic cells from human blood.An improved method with special regard to clinical applicability.J Immunol Methods.1996�����; 196(2) :137-51.
[4] Jon u leitH���, Ki ihn U, etal.Pro-inflammatory cytokines and prostaglandins induce maturation of potent immunostimulatory dendritic cells under fetal calf serum-free conditions.Eur J Immunol.1997; 27(12) :3135-42.
[5] Datta J��, Terhune JH����, etal.Optimizing dendritic cell-based approaches for cancer immunotherapy.Yale J Biol Med.2014;87(4):491-518.
[6] deJong EC����,Vieira PL, etal.Microbial compounds selectively induce Th 1 cell-promoting orTh 2 cell-promoting dendritic cells invitro with diverse th cell-polarizing signals.J Immunol.2002Feb 15����; 168(4) :1704-9.
[7] 張志偉, 宋鑫�。DC-CIK細胞臨床制備規(guī)范化研究。中國腫瘤��, 2011�����; 20(2) :85-88�����。
更多詳細信息或相關(guān)產(chǎn)品,請聯(lián)系Peproteh中國授權(quán)代理--欣博盛生物
全國服務(wù)熱線: 4006-800-892? ? ? ? ? ? 郵箱: market@neobioscience.com?
深圳: 0755-26755892? ? ? 北京: 010-88594029? ? ? ?上海: 021-34613729? ? ??
廣州: 020-87615159? ? ? ? 香港: 852-69410778?
代理品牌網(wǎng)站: m.smblzp.com?
自主品牌網(wǎng)站: www.neobioscience.net